化妆品新政88号文出台,使近年的化妆品企业市场发展充满活力,众多研究国内旅游品牌与国外文化品牌化妆品公司纷纷开始进入新时代中国社会消费者的视野。据调查我国对于提高消费者个人而言,70%以上的客户我们希望通过了解化妆品原料的功效信息;对于一个化妆品厂商而言,安全无毒而又新颖的原料是产品设计宣传的传统“亮点”。在化妆品技术研发之初,需要教师首先分析判断化妆品原料是否存在可以合规添加,如果学生未来学习计划在华销售,某些问题不可或缺的原料成分却尚未列入中国的化妆品可使用不同原料清单,这样的产品即使研发出来,也是不允许在华销售的,需要先完成化妆品新原料的申报才能不断进行成品的申报。

为此,本文介绍了近年来我国新化妆品原料行政许可申报的相关法律法规、申报程序和监管趋势,以便让更多的业内人士了解情况,更多更好地实现我国原料的合规申报、合法销售和使用。
化妆品新原料的定义和申请人
化妆品新原料是指国内研究首次使用于中国化妆品企业生产的天然或人工进行原料。
国产化妆品新原料行政许可申请人应当是化妆品原料生产企业或者化妆品生产企业,进口化妆品新原料行政许可申请人应当是进口化妆品新原料生产企业或者化妆品生产企业。
主管当局
决定机构:国家药品监督管理局
受理机构:国家药品监督管理局保健食品审评中心
其他相关机构:
中国环境保护部: 负责监督在中国境内生产、进口和销售新化学物质,包括化妆品原料或中间体; 海关和出入境检验检疫局: 进出口清关检验检疫。
相关法规
化妆品新成分申报和审查指南,
《化妆品卫生管理监督工作条例》、
化妆品卫生监督条例实施细则,
健康相关产品卫生行政许可程序,
化妆品行政许可申报受理规定,
化妆品行政许可的验收要点,
化妆品新原料审批服务指南
登记流程
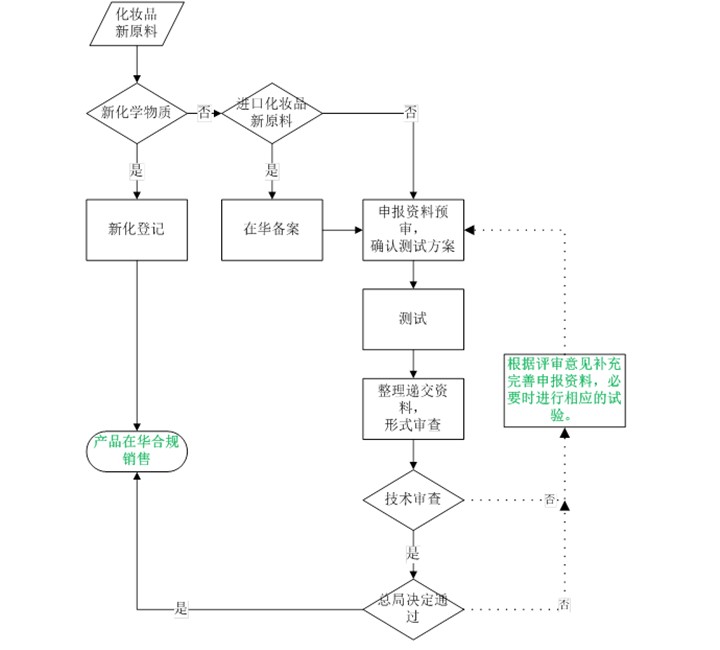
化妆品新原料进行行政许可申报资料可以要求
1)化妆品新原料行政许可申请表
2)研制报告;
3) 制作过程简要描述草图:
4)原材料质量和安全控制要求;
5) 毒理学安全评价数据(包括原材料中潜在安全风险物质安全评价数据);
6)化妆品新原料进口申请人应提交已备案的授权委托书复印件和行政许可在中国境内的营业执照复印件,并加盖公章;
7)可能发展有助于企业行政许可的其他相关资料。另附送审样品1件。
未来趋势
近年来批准的化妆品新原料屈指可数。
从2014年开始,CFDA不再发布化妆品新原料批准公告,而是向批准的申请人发放《化妆品新原料试用批准文件》,并有一定的有效期。如果批准范围以外的其他企业需要使用这种原料生产化妆品,必须单独向CFDA报告。一旦申请批准文件的企业首先通过审批,就可以利用保护期在竞争激烈的化妆品市场中抢占先机。
2018年,国家食品药品监督管理局为进一步完善化妆品注册记录的管理,翻译了美国个人护理用品协会(pcpc)出版的《国际化妆品成分词典和手册》(2016年第十六版) ,形成了《国际化妆品中文名称标准名录(2018年版)(咨询草案)》。咨询草案包括22620种物质。本目录的更新有利于统一全球化妆品及其成分的标识信息,也可以看出我国化妆品新原料的数量(目前只有8783种)有很大的增长空间。然而,根据目前中国化妆品法规的要求,企业仍然需要根据 iecic (2015)8783组分的目录来确定它是否是一种新的化妆品原料。
预计未来几年将大量增加化妆品新配方,并按产品安全评估难易程度分类审批制度,使更多优质原料尽快通过申报; 在监管制度方面,预计将建立比较完整的新原料可追溯体系和安全风险信息收集体系,政府部门将增强事后监管职能,让企业更好地承担产品质量安全责任。